下面我将详细解释这个过程,并补充其他可能的原因。
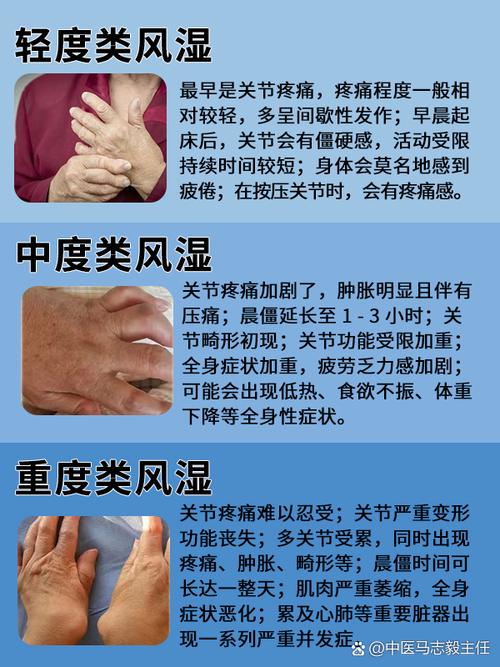
(图片来源网络,侵删)
核心原因:慢性病性贫血 / 炎症性贫血
这是RA患者贫血最主要、最常见的原因,占了大约80%的病例,其根本原因在于长期的、系统性的炎症反应。
发病机制详解:
-
铁代谢紊乱(“功能性缺铁”)
- 正常铁代谢: 铁是制造血红蛋白的关键原料,健康状态下,食物中的铁在肠道被吸收,进入血液后,由一种叫做转铁蛋白的蛋白质“搭载”并运送到骨髓,供红细胞制造使用,用不完的铁则以“铁蛋白”的形式储存在肝脏、脾脏等器官里。
- RA时的铁代谢异常: RA患者的炎症因子(尤其是白细胞介素-6, IL-6)会“劫持”这一正常过程。
- 铁被“扣押”在储存器官: 炎症因子会刺激肝脏产生一种叫做铁调素的物质,铁调素的作用就像一个“交通警察”,它命令肠道减少铁的吸收,并命令储存铁的器官(如肝脏)“锁住”铁,不让它释放到血液中。
- 结果: 尽管患者体内的铁总量可能是正常的,甚至充足的,但这些铁却被困在了仓库里,无法被骨髓利用,这就造成了“功能性缺铁”——骨髓缺铁,但血清铁(血液中的铁)和总铁储备却是低的,骨髓因缺乏原料而无法高效制造红细胞,从而导致贫血。
-
红细胞寿命缩短
- 炎症环境本身对红细胞是有毒性的,炎症产生的自由基和代谢产物会损伤红细胞膜,使其变得脆弱,容易被破坏。
- 炎症也可能激活免疫系统,产生一些抗体或免疫复合物,附着在红细胞表面,使其被提前清除。
- 正常红细胞的寿命约为120天,而在RA患者中,这个时间可能会显著缩短,红细胞破坏的速度加快,而骨髓的生成速度又跟不上,贫血自然会发生。
-
骨髓造血功能受抑
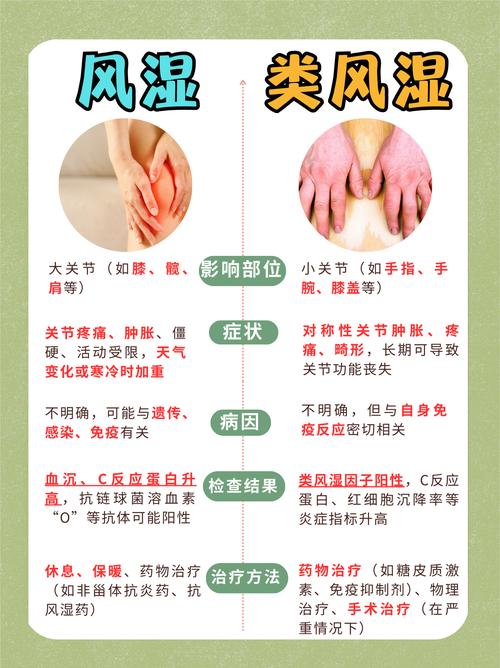 (图片来源网络,侵删)
(图片来源网络,侵删)- 长期、高水平的炎症因子(如TNF-α, IL-1, IL-6等)会直接抑制骨髓中造血干细胞的增殖和分化,使其产生红细胞的效率下降。
- 这就像一个工厂,虽然原材料(铁)的供应渠道被部分堵塞,同时工厂的生产线也因为“罢工”(炎症抑制)而效率低下,导致最终产品(红细胞)产量不足。
RA患者的贫血,是一个“原料供应受阻 + 产品消耗加快 + 生产效率低下”的“三重打击”结果,核心驱动力就是失控的炎症。
其他可能的原因
除了上述最主要的慢性病性贫血,RA患者还可能因为其他原因贫血:
-
药物引起的贫血
- 非甾体抗炎药: 如布洛芬、萘普生等,长期或大剂量使用可能刺激胃肠道,导致消化道出血,引起缺铁性贫血,这是临床上需要鉴别的重要原因。
- 改善病情抗风湿药: 甲氨蝶呤、来氟米特等药物也可能引起骨髓抑制,导致白细胞、血小板和红细胞全面减少,但相对少见。
-
自身免疫性溶血性贫血
这是一种比较严重的并发症,在某些情况下,RA的异常免疫系统可能会产生攻击自身红细胞的抗体(称为“温抗体”),导致红细胞被大量破坏,发生溶血性贫血,这种贫血通常比较严重,进展快。
-
营养缺乏性贫血
- 缺铁性贫血: 除了NSAIDs引起的出血,如果患者因关节疼痛、活动受限导致食欲不振,或饮食结构不合理,也可能导致铁摄入不足。
- 缺乏维生素B12或叶酸: 这两种物质也是红细胞成熟所必需的,虽然不常见,但如果患者存在吸收障碍或饮食不均衡,也可能发生。
-
肾脏疾病(肾性贫血)
- 长期、严重的RA可能并发肾脏淀粉样变性或其他类型的肾损伤,肾脏是分泌促红细胞生成素的器官,这种激素是骨髓制造红细胞的“总司令”,一旦肾功能受损,EPO分泌不足,也会导致贫血。
如何区分和治疗?
- 诊断: 医生会通过血常规(看红细胞、血红蛋白、平均红细胞体积等指标)和铁代谢检查(看血清铁、总铁结合力、铁蛋白、转铁蛋白饱和度等)来区分是哪种类型的贫血,典型的慢性病性贫血会表现为“血清铁低、总铁结合力低、铁蛋白正常或升高”的特点。
- 治疗:
- 根本治疗: 最关键的是积极控制RA本身的炎症活动,使用改善病情抗风湿药、生物制剂(如TNF-α抑制剂)等有效控制病情后,贫血通常也会随之改善。
- 对症治疗:
- 对于严重的慢性病性贫血,如果血红蛋白过低,医生可能会考虑使用促红细胞生成刺激剂来模拟EPO的作用,刺激骨髓造血。
- 绝对不要自行补铁! 对于慢性病性贫血,盲目补铁不仅无效,反而可能为细菌等病原体提供“养料”,加重感染风险,只有在明确合并了缺铁性贫血时,才需要在医生指导下补铁。
- 如果是药物或溶血等原因引起的贫血,则需要针对具体原因进行相应处理。
类风湿关节炎患者的贫血是其系统性炎症的一个“副产品”,是疾病活动度的一个重要标志,治疗贫血的关键在于控制好类风湿关节炎本身。




